| CAS |
915019-65-7 |
| English Name |
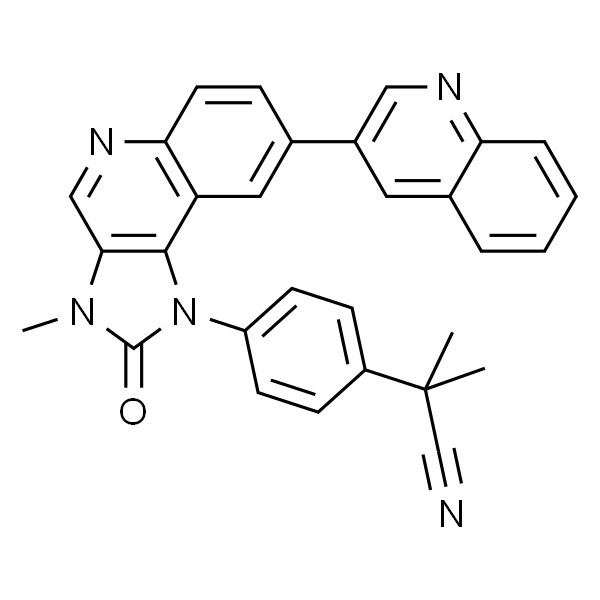
Dactolisib |
| Synonyms |
2-甲基-2-[4-[3-甲基-2-氧代-8-(喹啉-3-基)-2,3-二氢咪唑并[4,5-c]喹啉-1-基]苯基]丙腈;BEZ235; |
| Molecular Formula |
C30H23N5O |
| Molecular Weight |
469.55 |
| Solubility |
Soluble in DMSO |
| Purity |
≥98% |
| Appearance |
White to off-white Solid |
| Storage |
Powder:2-8℃,2 years;Insolvent(Mother Liquid):-20℃,6 months;-80℃,1 year |
| EC |
EINECS 1312995-182-4 |
| MDL |
MFCD00005880 |
| SMILES |
CN(C1=C2C3=CC(C4=CC5=CC=CC=C5N=C4)=CC=C3N=C1)C(N2C6=CC=C(C=C6)C(C)(C#N)C)=O |
| Target Point |
PI3K;mTOR |
| Passage |
PI3K/Akt/mTOR |
| Background |
BEZ235 is a dual pan-class I PI3K and mTOR inhibitor. |
| Biological Activity |
BEZ235 是一种双重的 pan-class I PI3K 和 mTOR 抑制剂,作用于 p110α/γ/δ/β 和 mTOR,IC50 分别为 4 nM/5 nM/7 nM/75 nM 和 20.7 nM。BEZ235 抑制 mTORC1 和 mTORC2[1-3]。 |
| In Vitro |
Dactolisib以ATP竞争方式有效抑制PI3K。 Dactolisib(250nM)显著降低mTOR活化激酶p70S6K的磷酸化水平。 Dactolisib还导致S235/S236P-RPS6水平降低,IC50为6.5 nM,表明Dactolisib可直接抑制mTOR激酶,因为mTOR的激酶结构域与IA类PI3K高度同源。 。使用生化mTOR K-LISA测定法(IC50,20.7nM)确认Dactolisib对mTOR的活性[1]。 Dactolisib对HCT116,DLD-1和SW480细胞系的IC50分别为14.3±6.4,9.0±1.5和12.0±1.6 nM [2]。 |
| In Vivo |
Dactolisib(45 mg/kg,口服)治疗在散发性PIK3CA野生型CRC的GEM模型中诱导结肠肿瘤消退[2]。通过口服强饲法将Dactolisib(45mg/kg)给予MENX大鼠(每组n = 2),并在处理后1或6小时处死动物。与PEG处理的大鼠相比,P-AKT和P-S6的免疫染色显示在给予Dactolisib后6小时,两种蛋白质,特别是P-S6的显著减少。在治疗后6小时,Dactolisib处理的大鼠的垂体腺瘤具有与安慰剂治疗的大鼠的肿瘤显著不同的蛋白质组学特征[3]。 |
| Cell Experiment |
HCT116(PIK3CA突变体; H1047R的激酶结构域),DLD-1(PIK3CA突变体; E545K的螺旋结构域)和SW480(PIK3CA野生型)人CRC细胞系(ATCC)和同基因DLD-1 PIK3CA突变体和野生型将细胞维持在含有10%FBS和1×青霉素/链霉素的DMEM中。以不同的初始密度接种细胞(HCT116:3,000个细胞/孔,DLD-1:5,500个细胞/孔,SW480:4,500个细胞/孔,DLD-1 PIK3CA突变体:7,000个细胞/孔,和DLD-1 PIK3CA野生型):9,000个细胞/孔)以解释差异生长动力学。 16小时后,将细胞与浓度增加的BEZ235(10,100,1000nM)一起温育,每24小时更换含药物的生长培养基。使用比色MTS测定CellTiter 96 AQueous One Solution Cell Proliferation Assay,在初始接种后16小时和药物治疗开始后48小时评估细胞活力。药物处理后的细胞活力标准化为也生长48小时的未处理细胞的细胞活力。使用GraphPad Prism 5 [2]中的4参数非线性回归计算IC 50值。 |
| Animal Experiment |
小鼠[2]将携带肿瘤的Apc CKO小鼠随机分配到单独使用对照载体(n = 8)或45 mg/kg体重BEZ235在10%1-甲基-2-吡咯烷酮/ 90%PEG 300中治疗(n = 8)每日口服强饲28天。基于文献选择治疗剂量,表明40-50mg/kg体重BEZ235有效地治疗小鼠肿瘤模型而没有副作用。基于在Dactolisib施用后1小时显示最大组织浓度的药代动力学研究,在最终治疗剂量后1小时处死荷瘤小鼠。使用卡尺(宽×长×高)评估结肠肿瘤体积,收集肿瘤用于蛋白质印迹分析和免疫组织化学。使用大鼠[3] MENX影响的大鼠。在MENX大鼠中测试三剂BEZ235:20,30和45mg/kg。由于两次较高剂量在治疗10天后导致体重减轻> 10%,因此20mg/kg的剂量用于进一步研究。对于MRI研究,在7至8个月大的MENX受影响的大鼠(具有相当大的腺瘤但仍具有良好的一般健康状况)用口服强饲法每日施用BEZ235(20mg/kg)或安慰剂(PEG)治疗14天。 |
| Kinase Experiment |
PI3Kα,β和δ蛋白由p85 NH2的iSH2结构域组成,其末端与全长蛋白p110蛋白融合,但α也不包含最后20个氨基酸。 PI3Kγ作为其前144个氨基酸缺失的全长蛋白质产生。将所有构建体与COOH-末端His标签融合以便于纯化,然后克隆到pBlue-Bac4.5(对于α,β和δ同种型)或pVL1393(对于γ同种型)质粒中。然后使用供应商推荐的方法用BaculoGold WT基因组DNA共转染不同载体以产生相应的重组杆状病毒和蛋白质。使用Kinase-Glo测定法测试化合物对PI3K的活性。激酶反应在384孔黑色板中完成。每孔加载50nL测试项目(在90%DMSO中)和5μL反应缓冲液[10mM Tris-HCl(pH 7.5),50mM NaCl,3mM MgCl 2,1mM DTT和0.05%CHAPS] 10μg/ mL PI底物(L-α-磷脂酰肌醇; Avanti极性脂质;在3%辛基葡萄糖苷中制备)和PI3K蛋白(分别为10,25,10和150 nM的p110α,p110β,p110δ和p110γ))然后添加。通过加入在反应缓冲液中制备的5μL1μMATP开始反应,并且运行60(对于p110α,p110β和p110δ)或120分钟(对于p110γ)并且随后通过添加10μL激酶终止反应。 -Glo缓冲区。然后在Synergy 2读数器中读取平板用于发光检测[1]。 |
| Data Literature Source |
[1]. Maira SM,et al. Identification and characterization of NVP-BEZ235,a new orally available dual phosphatidylinositol 3-kinase/mammalian target of rapamycin inhibitor with potent in vivo antitumor activity. Mol Cancer Ther,2008,7(7),1851-1863.
[2]. Roper J,et al. The dual PI3K/mTOR inhibitor NVP-BEZ235 induces tumor regression in a genetically engineered mouse model of PIK3CA wild-type colorectal cancer. PLoS One,2011,6(9),e25132.
[3]. Lee M,et al. Targeting PI3K/mTOR Signaling Displays Potent Antitumor Efficacy against Nonfunctioning Pituitary Adenomas. Clin Cancer Res. 2015 Jul 15;21(14):3204-15 |
| Unit |
Bottle |
| Specification |
10mg 25mg 50mg |

 English
English
 中文
中文

 Manual Download
Manual Download

